Traduzione di How did scientists manage to develop safe COVID-19 vaccines in just ten months?, pubblicato su Gavi, the Vaccine Alliance
I vaccini anti-covid approvati di recente e quelli che hanno raggiunto l’ultimo stadio della sperimentazione sono stati sviluppati più velocemente di qualsiasi altro vaccino contro una nuova malattia. In che modo gli scienziati sono riusciti in questa incredibile impresa? Gli insegnamenti tratti dalla ricerca potrebbero consentire uno sviluppo più rapido anche dei vaccini futuri?
Prima del Covid-19, generalmente ci volevano dieci anni o più per sviluppare un vaccino e renderlo accessibile a tutta la popolazione. Tuttavia ci sono state alcune eccezioni alla regola: il primo vaccino contro la poliomielite sviluppato da Jonas Salk è stato messo a punto in soli sei anni e, più recentemente, un vaccino contro il virus Zika, in soli sei mesi e mezzo dall’inizio delle sperimentazioni sull’uomo. Anche i vaccini contro l’influenza H1N1, nel 2009 sono stati resi disponibili dopo 6 mesi dall’inizio della pandemia. Allo stesso modo, i vaccini anti-covid in fase avanzata di sperimentazione clinica, o in fase di commercializzazione, sono stati sviluppati in meno di un anno. Alcuni, comprensibilmente, si preoccupano per la rapidità della ricerca, ma, sebbene alcuni processi di sviluppo siano stati condensati, ciò non significa che la sicurezza del vaccino sia stata compromessa. Questo significa invece che, in questo caso, decisori politici, collaborazione internazionale e impegno sono stati elementi fondamentali per ottenere un vaccino in tempi record.
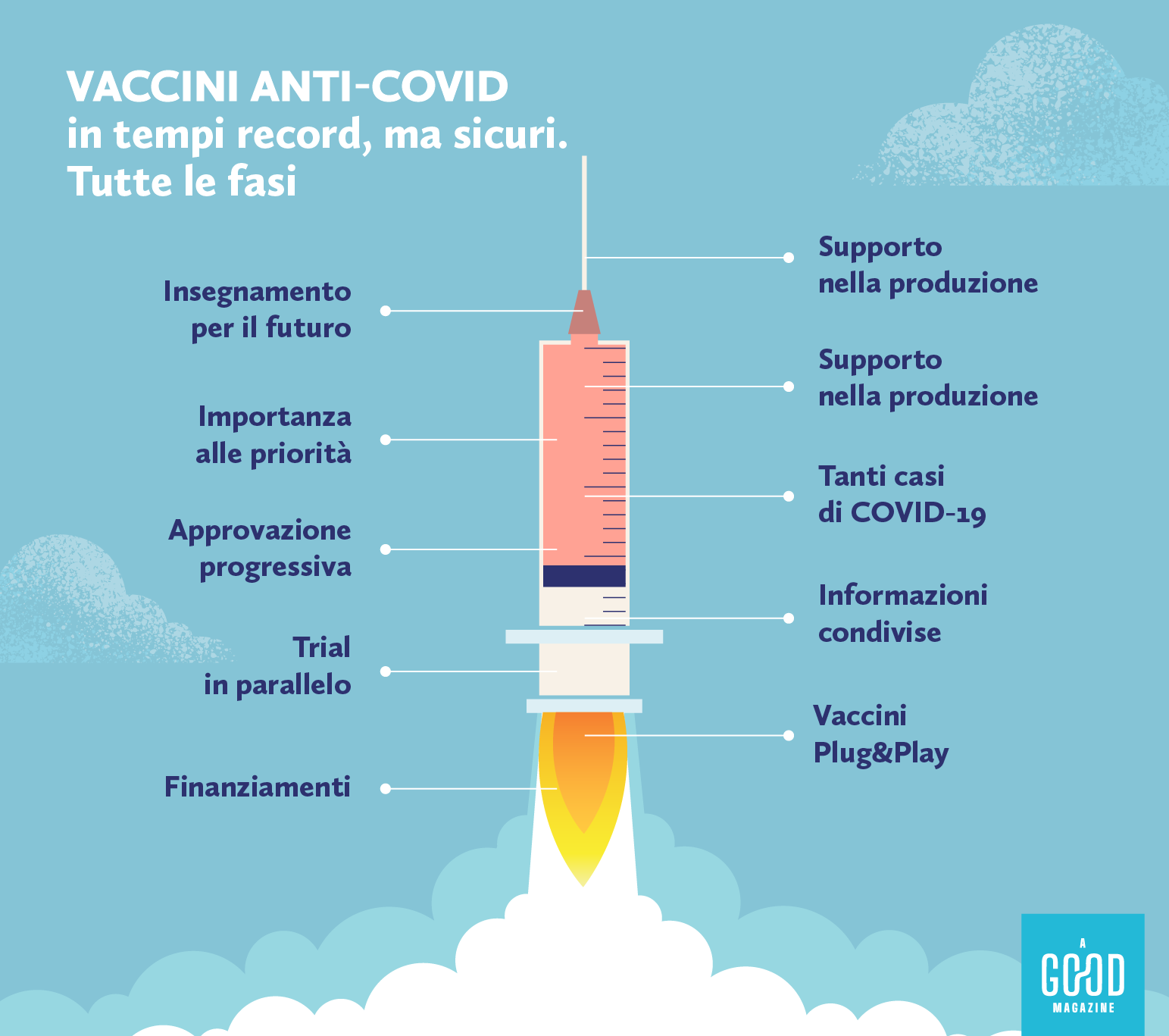
Finanziamenti
Data la pressante domanda globale di vaccini sicuri ed efficaci anti-covid, per il loro sviluppo e la loro produzione sono stati necessari consistenti finanziamenti da parte sia degli Stati che dei privati. Con COVAX – alleanza internazionale di 190 paesi ed economie -, per esempio, i governi hanno condiviso alcuni dei rischi finanziari associati alla scalabilità e alla produzione di grandi volumi di vaccini, già prima della loro autorizzazione. Tali finanziamenti hanno fornito ai ricercatori le risorse necessarie per le sperimentazioni cliniche e hanno reso possibile aumentare la capacità di produzione delle aziende farmaceutiche con molto anticipo.
Vaccini plug & play
L’uso di tecnologie come l’RNA messaggero e l’impiego dei vaccini vettoriali sono altri strumenti che hanno facilitato il rapido sviluppo dei vaccini anti-covid. Sia il vaccino Pfizer/BioNTech che molti di quelli attualmente in fase 3 – incluso il vaccino di AstraZeneca/Università di Oxford -, sono sistemi plug & play. Ciò significa che, una volta identificato un antigene adatto (una molecola che innesca una risposta immunitaria), la sua sequenza di DNA o RNA può essere immediatamente inserita in una piattaforma pre-convalidata (in questo caso, in un pezzo di RNA o nel genoma di un virus del raffreddore comune disattivato) per ottenere un nuovo vaccino.
Iniettato nel nostro corpo, il vaccino rilascia le informazioni genetiche al meccanismo di produzione proteica delle nostre cellule, inducendole a produrre gli antigeni e innescando, quindi, una risposta immunitaria al virus.
Il fatto che queste tecnologie fossero già in fase di sviluppo per contrastare altri virus ha indubbiamente aiutato. Ciò ha infatti permesso di sviluppare i prototipi dei vaccini in poco tempo, di sfruttare i dati sulla sicurezza dei vaccini esistenti, di utilizzare i processi produttivi già collaudati per accelerare la produzione e ridurre i costi.
Informazioni condivise
Identificare un antigene adatto per innescare una risposta immunitaria è un passaggio cruciale da cui dipendono tutti i passaggi successivi. Gli antigeni potrebbero includere componenti che si trovano sul guscio esterno dei virus, o altre proteine virali confezionabili in modo da farle sembrare più interessanti per il sistema immunitario. Una volta identificati gli antigeni più promettenti, questi vengono testati sugli animali per studiarne la sicurezza e la capacità di innescare una risposta immunitaria abbastanza forte. Soltanto per ultimare questi primi due passaggi, solitamente c’era bisogno di 5-6 anni di ricerca.
Nel caso di alcuni dei nuovi vaccini a RNA, invece, i primi antigeni per il Covid-19 sono stati mappati poche ore dopo la rivelazione del genoma del Coronavirus da parte degli scienziati cinesi. Anche la condivisione di informazioni sugli antigeni dei Coronavirus correlati responsabili della SARS e della MERS ha aiutato molto. Insieme, tutte queste intuizioni hanno accelerato il processo di sviluppo di anni.
Trial in parallelo
La fase successiva è costituita dalle sperimentazioni del vaccino sull’uomo. Queste, di solito vengono effettuate in sequenza: la fase 1 verifica la sicurezza del vaccino su un piccolo numero di persone; la fase 2 estende l’esame a più persone; la fase 3, coinvolge migliaia o decine di migliaia di persone. Il completamento di tutte le fasi può richiedere fino a un decennio, non per la sperimentazione in sé, ma a causa dei tempi necessari per la stesura delle domande di sovvenzione, dell’ottenimento dell’approvazione normativa per le sperimentazioni, dalla negoziazione con i produttori e del reclutamento dei partecipanti alla sperimentazione. Nel caso dei vaccini anti-covid, invece, è stato possibile avviare due fasi in contemporanea, accelerando sensibilmente il processo. Inoltre, i social media e la volontà di contenere il contagio da parte delle persone hanno consentito ai ricercatori di individuare volontari per i trial in poco tempo.
L’esecuzione di varie fasi praticamente in parallelo ha anche permesso ai ricercatori di apprendere più cose in minor tempo, individuando diversi gruppi di rischio durante il processo per costruire un profilo più completo dell’efficacia dei vaccini in diverse fasce demografiche. In più, lo studio è stato condotto in numerosi siti di sperimentazione in tutto il mondo, rendendo ancora più facile reclutare volontari per i trial nelle aree in cui c’erano più contagi in tempo reale. Tutto questo ha comportato una riduzione complessiva del tempo necessario per valutare l’efficacia del vaccino.
Tanti casi di Covid-19
Le sperimentazioni cliniche possono richiedere anni e anni in caso di malattie rare. Solitamente occorre molto tempo per stabilire se chi ha ricevuto il vaccino ha sviluppato gli anticorpi contro la malattia. Nel caso dell’Ebola, per esempio, è stato particolarmente difficile fare tale constatazione proprio per il numero ridotto di contagiati, fino all’epidemia di Ebola nell’Africa occidentale del 2014-2016. Nel caso del Covid-19, invece, i numerosi contagiati, anche in paesi con infrastrutture idonee per condurre studi clinici randomizzati, se da un lato hanno rappresentato una tragedia per l’umanità, ,dall’altro hanno permesso di ottenere un esito delle sperimentazioni cliniche in pochissimo tempo.
Approvazione progressiva
Il processo di approvazione normativa è costoso e rischioso per le aziende farmaceutiche, per questo le agenzie regolatorie richiedono dati dettagliati e completi sui vaccini prima di approvarli. Di solito, quindi, le aziende farmaceutiche aspettano di avere tutti i dati su un vaccino per inviare alle agenzie regolatorie una documentazione completa. Tuttavia, a causa dell’emergenza sanitaria, molte agenzie regolatorie hanno introdotto un processo di “revisione continua” per i potenziali vaccini anti-covid, consentendo alle aziende di presentare i dati sull’efficacia non appena fossero disponibili, anche in più volte. L’obiettivo è accorciare i tempi di valutazione e approvazione per un farmaco o un vaccino.
Supporto nella produzione
Dato che un singolo polo produttivo può costare più di mezzo miliardo di dollari e che un potenziale vaccino ha meno di 1/5 possibilità di successo (anche se arrivato ai trial clinici), i produttori sono comprensibilmente cauti nel fare investimenti così consistenti, almeno fino a quando non sono certi di avere fra le mani un prodotto approvato e commerciabile. Tuttavia, rimandare la costruzione o il potenziamento dei siti produttivi dei vaccini e della filiera di approvvigionamento necessaria per la loro distribuzione crea ulteriori ritardi che costano vite umane. Condividendo parte dei rischi con i produttori, Gavi e i suoi partner (COVAX, The Coalition for Epidemic Preparedness Innovations e l’Organizzazione Mondiale della Sanità) hanno consentito ai produttori di avviare di iniziare a produrre i vaccini in tempi ragionevoli. Ciò significa che le persone in tutto il mondo dovrebbero avere accesso ai vaccini il prima possibile.
Importanza delle priorità
Un elemento chiave alla base di questi incredibili progressi è la priorità che tutte le persone coinvolte nello sviluppo, nei test, nella valutazione e nella revisione dei vaccini hanno dato a questo lavoro. I vaccini anti-covid sono un eccellente esempio di cos’è possibile ottenere quando in molti ci si impegna con la massima dedizione verso un obiettivo comune.
Insegnamento per il futuro
Con la pandemia abbiamo capito che è possibile sviluppare, testare e rivedere più vaccini sicuri ed efficaci contro una nuova malattia in meno di un anno. Risultati così incoraggianti da più di un vaccino fanno ben sperare, sia per la fine della pandemia, sia per lo sviluppo di eventuali vaccini contro altre nuove malattie che potrebbero tramutarsi in una prossima epidemia. Questo, solo se facciamo tesoro degli insegnamenti di questo periodo straordinario.



Lascia il tuo commento